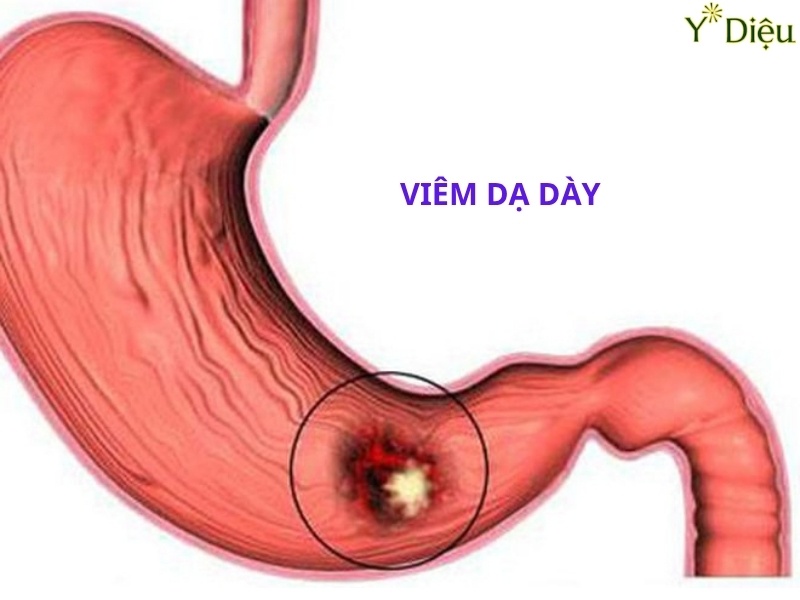
Virus HP Dạ Dày Phương Pháp Điều Trị Và Cách Ngăn Ngừa
Khái Niệm Và Đặc Điểm Của Virus HP Dạ Dày
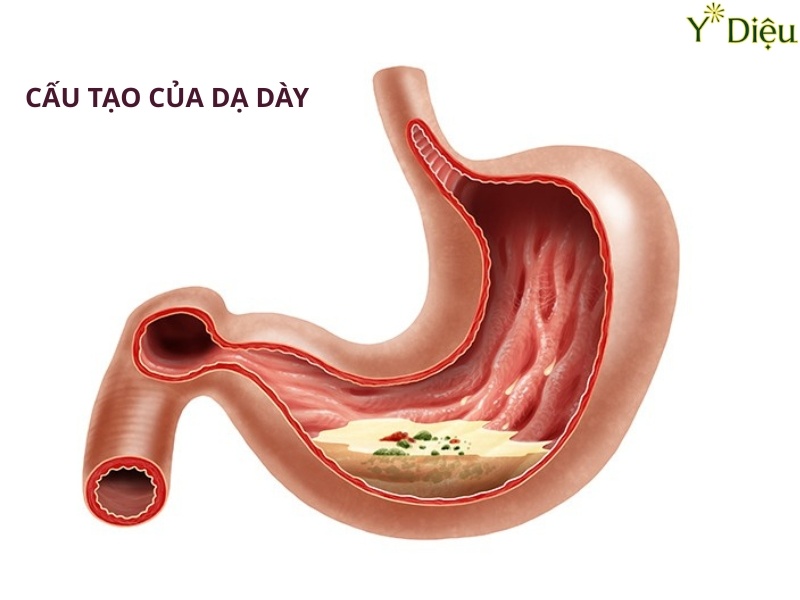
Virus HP dạ dày thực chất là cách gọi phổ biến trong cộng đồng dành cho Helicobacter pylori (H. pylori), một loại vi khuẩn gram âm, hình xoắn ốc, có khả năng sinh tồn và phát triển mạnh mẽ trong môi trường acid khắc nghiệt của dạ dày người. Vi khuẩn này được phát hiện lần đầu tiên vào năm 1982 bởi hai nhà khoa học người Úc là Barry Marshall và Robin Warren, mở ra một bước ngoặt lớn trong hiểu biết về các bệnh lý dạ dày, đặc biệt là viêm loét dạ dày-tá tràng và ung thư dạ dày.
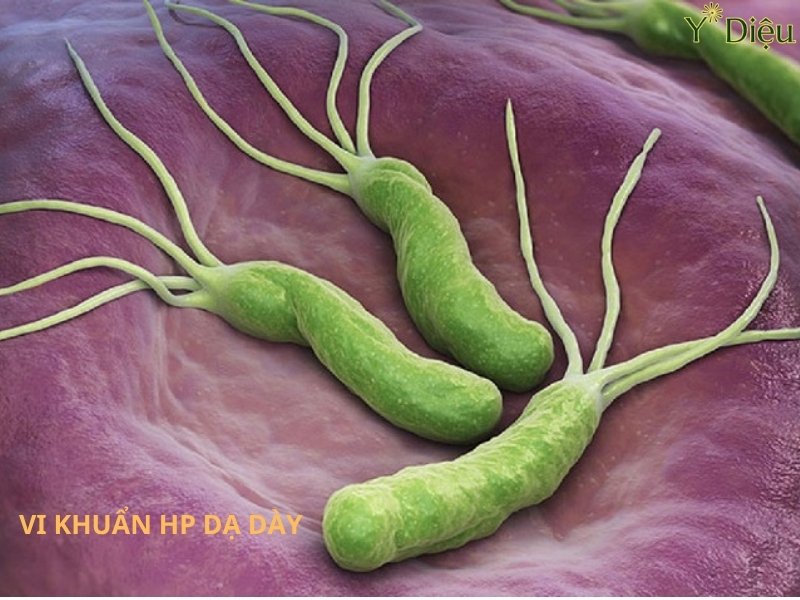
Virus HP dạ dày là một loại vi khuẩn gram âm, hình xoắn ốc
H. pylori là một trong những vi sinh vật gây bệnh phổ biến nhất trên thế giới, với tỷ lệ nhiễm lên tới 50% dân số toàn cầu. Tỷ lệ này đặc biệt cao ở các quốc gia đang phát triển, nơi điều kiện vệ sinh và nguồn nước sạch còn hạn chế. Sự lây nhiễm chủ yếu diễn ra qua đường tiêu hóa, thông qua tiếp xúc với nước, thực phẩm hoặc dụng cụ ăn uống bị nhiễm khuẩn, cũng như qua tiếp xúc gần gũi giữa các thành viên trong gia đình.
Đặc điểm hình thái và cấu trúc của H. pylori
H. pylori có hình dạng xoắn ốc đặc trưng, dài khoảng 2,5-5,0 μm và rộng 0,5-1,0 μm. Vi khuẩn này di chuyển linh hoạt nhờ 4-6 lông roi ở một đầu, giúp chúng dễ dàng xuyên qua lớp nhầy bảo vệ niêm mạc dạ dày. Cấu trúc vách tế bào của H. pylori thuộc loại gram âm, với lớp màng ngoài chứa lipopolysaccharide (LPS) đóng vai trò quan trọng trong việc bảo vệ vi khuẩn khỏi các yếu tố tấn công từ môi trường và hệ miễn dịch.
- Hình thái: Xoắn ốc, có thể biến đổi thành dạng cầu khi gặp điều kiện bất lợi.
- Lông roi: Tạo điều kiện cho vi khuẩn di chuyển trong môi trường nhầy đặc biệt của dạ dày.
- Gram âm: Vách tế bào mỏng, có lớp màng ngoài chứa LPS.
Cơ chế sinh tồn trong môi trường acid dạ dày
Một trong những đặc điểm nổi bật nhất của H. pylori là khả năng tồn tại trong môi trường acid mạnh của dạ dày (pH 1-2). Điều này đạt được nhờ vào enzyme urease mà vi khuẩn tiết ra với hàm lượng rất cao. Urease xúc tác phản ứng thủy phân ure thành amoniac và carbon dioxide, trong đó amoniac có tác dụng trung hòa acid xung quanh vi khuẩn, tạo ra một vùng vi môi trường có pH trung tính, bảo vệ H. pylori khỏi tác động phá hủy của acid dịch vị.
- Enzyme urease: Trung hòa acid, tạo điều kiện thuận lợi cho vi khuẩn bám dính và phát triển.
- Khả năng bám dính: H. pylori sử dụng các protein bám dính đặc hiệu (adhesin) để gắn chặt vào tế bào biểu mô dạ dày, chống lại sự đào thải của nhu động dạ dày và lớp nhầy bảo vệ.
- Di chuyển linh hoạt: Lông roi giúp vi khuẩn xuyên qua lớp nhầy, tiếp cận gần hơn với bề mặt niêm mạc.
Cơ chế né tránh hệ miễn dịch và biến đổi kháng nguyên
H. pylori có khả năng biến đổi kháng nguyên bề mặt, giúp chúng tránh được sự phát hiện và tấn công của hệ miễn dịch. Ngoài ra, vi khuẩn còn tiết ra các yếu tố ức chế miễn dịch như protein VacA, CagA, giúp làm giảm hiệu quả của các tế bào miễn dịch tại chỗ. Sự tồn tại kéo dài của H. pylori trong dạ dày dẫn đến phản ứng viêm mạn tính, làm tổn thương niêm mạc và tăng nguy cơ phát triển các bệnh lý nghiêm trọng như loét dạ dày-tá tràng và ung thư dạ dày.
- Biến đổi kháng nguyên: Thay đổi cấu trúc bề mặt để tránh bị nhận diện.
- Ức chế miễn dịch: Tiết ra các protein làm giảm hoạt động của đại thực bào và lympho T.
- Gây viêm mạn tính: Kích thích sản xuất cytokine, làm tổn thương niêm mạc kéo dài.
Đặc điểm sinh học và độc lực
H. pylori sở hữu nhiều yếu tố độc lực giúp chúng tồn tại và gây bệnh hiệu quả trong cơ thể người:
- Urease: Trung hòa acid, bảo vệ vi khuẩn khỏi môi trường khắc nghiệt.
- CagA (Cytotoxin-associated gene A): Là một protein được mã hóa bởi gen cagA, có khả năng xâm nhập vào tế bào biểu mô dạ dày, làm thay đổi cấu trúc tế bào, thúc đẩy quá trình viêm và tăng nguy cơ ung thư hóa.
- VacA (Vacuolating cytotoxin A): Gây độc cho tế bào, tạo các không bào trong tế bào biểu mô, làm rối loạn chức năng tế bào và góp phần vào quá trình viêm loét.
- LPS (Lipopolysaccharide): Gây đáp ứng miễn dịch mạnh, làm tổn thương mô.
- Adhesin: Protein bám dính giúp vi khuẩn gắn chặt vào tế bào chủ.
Khả năng lây nhiễm và yếu tố nguy cơ
H. pylori lây truyền chủ yếu qua đường tiêu hóa, đặc biệt là qua nước uống, thực phẩm hoặc dụng cụ ăn uống bị nhiễm khuẩn. Ngoài ra, lây truyền từ người sang người qua tiếp xúc nước bọt, dịch nôn hoặc phân cũng được ghi nhận. Một số yếu tố nguy cơ làm tăng khả năng nhiễm H. pylori bao gồm:
- Điều kiện vệ sinh kém: Sử dụng nước không đảm bảo vệ sinh, thực phẩm sống hoặc chưa nấu chín kỹ.
- Môi trường sống đông đúc: Dễ lây lan trong gia đình hoặc cộng đồng nhỏ.
- Tiếp xúc gần với người nhiễm: Đặc biệt là trẻ em sống chung với người lớn bị nhiễm H. pylori.
- Yếu tố di truyền: Một số nghiên cứu cho thấy có sự liên quan giữa yếu tố di truyền và nguy cơ nhiễm H. pylori.
Vai trò của H. pylori trong bệnh lý dạ dày
Sự hiện diện kéo dài của H. pylori trong dạ dày là nguyên nhân chính gây ra các bệnh lý như viêm dạ dày mạn tính, loét dạ dày-tá tràng, và là yếu tố nguy cơ hàng đầu dẫn đến ung thư dạ dày. Cơ chế bệnh sinh chủ yếu liên quan đến phản ứng viêm mạn tính do vi khuẩn kích thích sản xuất các cytokine gây viêm, làm tổn thương và phá hủy lớp niêm mạc bảo vệ dạ dày.
- Viêm dạ dày mạn tính: Gây đau bụng, khó tiêu, buồn nôn kéo dài.
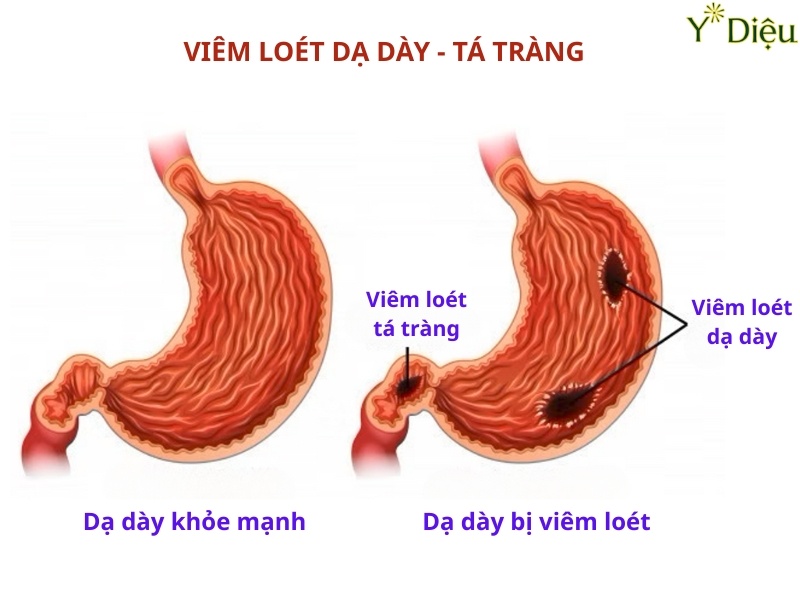
- Loét dạ dày-tá tràng: Do tổn thương lớp niêm mạc, hình thành ổ loét.
- Ung thư dạ dày: H. pylori là tác nhân gây ung thư dạ dày được Tổ chức Y tế Thế giới (WHO) xếp vào nhóm 1 các tác nhân gây ung thư ở người.
Khả năng kháng thuốc và thách thức trong điều trị
H. pylori ngày càng cho thấy khả năng kháng lại nhiều loại kháng sinh, đặc biệt là clarithromycin, metronidazole và levofloxacin. Điều này khiến việc điều trị tiệt trừ vi khuẩn trở nên khó khăn hơn, đòi hỏi các phác đồ phối hợp nhiều loại thuốc và kéo dài thời gian điều trị. Ngoài ra, việc tái nhiễm sau điều trị cũng là một vấn đề lớn, đặc biệt ở các khu vực có tỷ lệ nhiễm cao.
- Kháng thuốc: Do sử dụng kháng sinh không hợp lý, tự ý điều trị hoặc không tuân thủ phác đồ.
- Tái nhiễm: Nguy cơ cao ở trẻ em và các cộng đồng có điều kiện vệ sinh kém.
- Biến đổi di truyền: H. pylori có khả năng biến đổi gen nhanh, tạo ra các chủng kháng thuốc mới.
Cơ Chế Gây Bệnh Và Ảnh Hưởng Đến Sức Khỏe
Quá Trình Xâm Nhập Và Tác Động Lên Niêm Mạc Dạ Dày
Helicobacter pylori (H. pylori) là một loại vi khuẩn Gram âm, hình xoắn, có khả năng sinh tồn mạnh mẽ trong môi trường acid khắc nghiệt của dạ dày. Sau khi xâm nhập vào cơ thể qua đường tiêu hóa, H. pylori sử dụng các cấu trúc lông roi để di chuyển xuyên qua lớp nhầy bảo vệ niêm mạc dạ dày, tiếp cận và bám dính vào bề mặt các tế bào biểu mô niêm mạc. Quá trình bám dính này được hỗ trợ bởi các protein bề mặt đặc hiệu như BabA, SabA, giúp vi khuẩn gắn kết chặt chẽ với các thụ thể trên tế bào chủ.
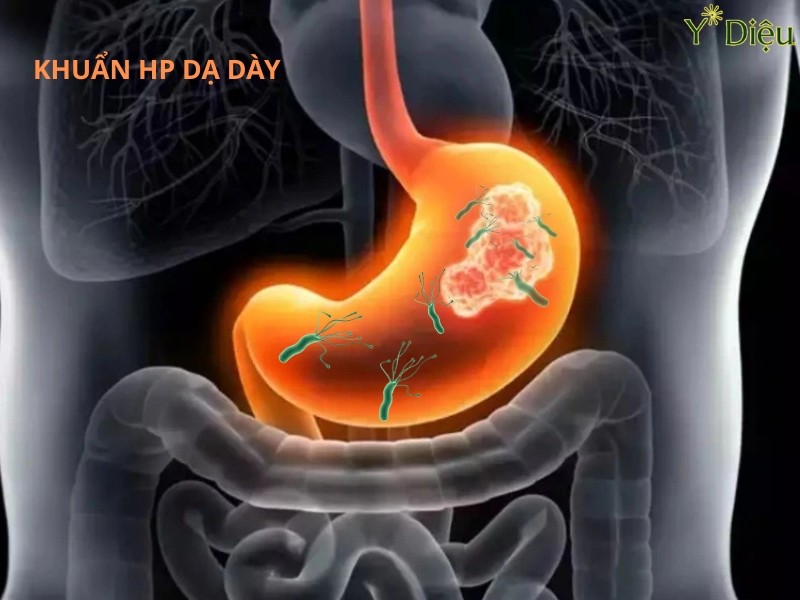
Quá trình xâm nhập và tác động lên niên mạc dạ dày
Một trong những đặc điểm sinh học quan trọng của H. pylori là khả năng tiết ra enzyme urease với nồng độ cao. Urease phân giải ure thành amoniac và carbon dioxide, trong đó amoniac có tác dụng trung hòa acid dạ dày xung quanh vi khuẩn, tạo ra một "vùng đệm" giúp H. pylori tồn tại và phát triển trong môi trường acid mạnh. Ngoài ra, vi khuẩn còn tiết ra các enzyme khác như protease và phospholipase, góp phần phá hủy cấu trúc protein và lipid của lớp nhầy bảo vệ, làm lộ ra lớp tế bào biểu mô bên dưới, tạo điều kiện thuận lợi cho vi khuẩn xâm nhập sâu hơn vào niêm mạc.
Đặc biệt, H. pylori còn sản xuất các độc tố mạnh như VacA (Vacuolating cytotoxin A) và CagA (Cytotoxin-associated gene A). VacA gây tổn thương trực tiếp lên tế bào biểu mô, tạo ra các không bào lớn trong tế bào, làm rối loạn chức năng tế bào và thúc đẩy quá trình chết tế bào theo chương trình (apoptosis). CagA, sau khi được tiêm vào tế bào chủ thông qua hệ thống tiết type IV, sẽ tác động lên các con đường tín hiệu nội bào, làm thay đổi hình thái, tăng sinh và khả năng di chuyển của tế bào, đồng thời kích thích mạnh mẽ phản ứng viêm.
Quá trình viêm mạn tính do H. pylori kích hoạt là kết quả của sự xâm nhập liên tục của các tế bào miễn dịch như bạch cầu trung tính, lympho bào T và B, đại thực bào vào vùng niêm mạc bị tổn thương. Các tế bào này giải phóng hàng loạt cytokine tiền viêm (IL-1β, IL-6, TNF-α, INF-γ), gây tổn thương thêm cho mô niêm mạc, phá vỡ hàng rào bảo vệ tự nhiên của dạ dày. Sự mất cân bằng giữa yếu tố bảo vệ và yếu tố tấn công dẫn đến phá hủy cấu trúc niêm mạc, hình thành các ổ loét, tăng nguy cơ xuất huyết tiêu hóa, thủng dạ dày và tiến triển thành các tổn thương ác tính.
Ngoài ra, H. pylori còn ảnh hưởng đến quá trình tiết acid dạ dày thông qua tác động lên tế bào G (tăng tiết gastrin) và tế bào D (giảm tiết somatostatin), gây rối loạn cân bằng acid-bazơ trong dạ dày. Hậu quả là bệnh nhân có thể xuất hiện các triệu chứng lâm sàng như:
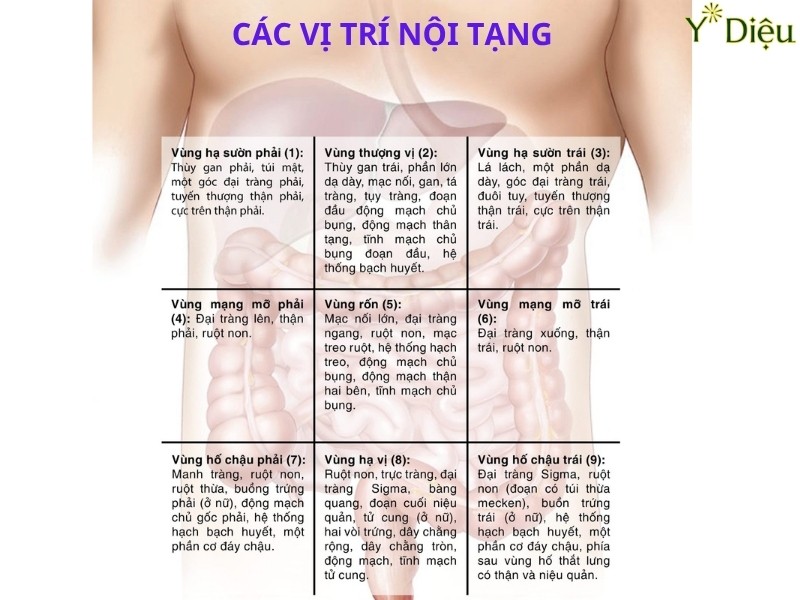
- Đau thượng vị: Đau âm ỉ hoặc dữ dội vùng trên rốn, thường tăng sau ăn hoặc khi đói.
- Đầy hơi, chướng bụng: Do rối loạn vận động dạ dày và tăng sinh khí trong lòng dạ dày.
- Buồn nôn, nôn: Kích thích niêm mạc và rối loạn nhu động tiêu hóa.
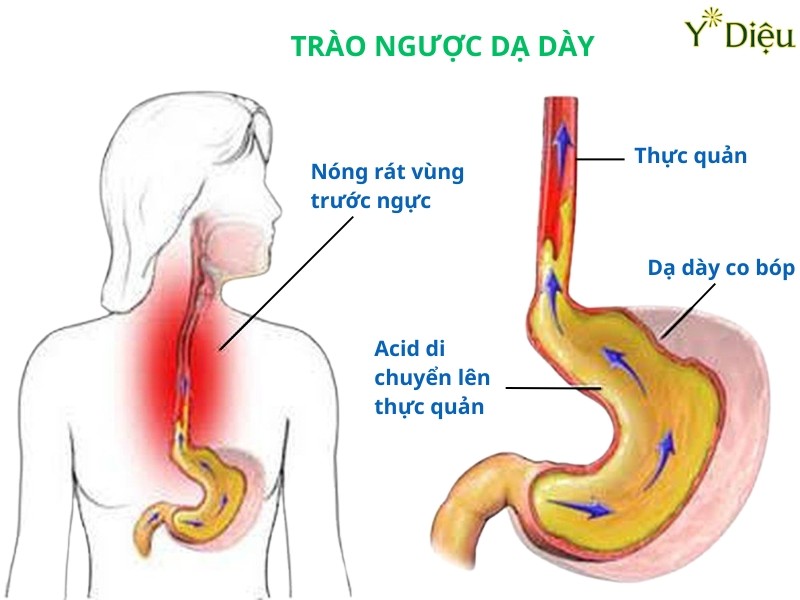
- Ợ nóng, ợ chua: Do tăng tiết acid và trào ngược dịch vị lên thực quản.
- Khó tiêu: Cảm giác no sớm, ăn không ngon miệng, khó chịu kéo dài.
Đáng chú ý, một tỷ lệ không nhỏ người nhiễm H. pylori không có triệu chứng rõ ràng (nhiễm không triệu chứng), nhưng vẫn tiềm ẩn nguy cơ cao phát triển các biến chứng nghiêm trọng về lâu dài, đặc biệt khi có các yếu tố nguy cơ phối hợp như di truyền, chế độ ăn uống, hút thuốc lá, lạm dụng rượu bia.
Biến Chứng Liên Quan Đến Virus HP Dạ Dày
Nhiễm H. pylori là nguyên nhân hàng đầu gây ra nhiều bệnh lý dạ dày - tá tràng, với các biến chứng nguy hiểm có thể đe dọa tính mạng nếu không được phát hiện và điều trị kịp thời. Các biến chứng phổ biến và cơ chế bệnh sinh liên quan bao gồm:
- Viêm dạ dày mạn tính: Viêm mạn tính do H. pylori là kết quả của quá trình kích hoạt liên tục hệ miễn dịch tại chỗ, dẫn đến tổn thương kéo dài của niêm mạc dạ dày. Tình trạng này làm giảm khả năng tái tạo của tế bào biểu mô, gây xơ hóa, teo niêm mạc và rối loạn chức năng tiết dịch vị. Bệnh nhân thường có triệu chứng đau âm ỉ vùng thượng vị, đầy bụng, khó tiêu kéo dài, đôi khi kèm theo xuất huyết nhẹ.
- Loét dạ dày - tá tràng: Sự phá hủy lớp nhầy bảo vệ và tổn thương trực tiếp tế bào biểu mô do enzyme và độc tố của H. pylori tạo điều kiện cho acid và pepsin tấn công sâu vào thành dạ dày hoặc tá tràng, hình thành các ổ loét. Loét có thể tiến triển thành xuất huyết tiêu hóa (nôn ra máu, đi ngoài phân đen) hoặc thủng dạ dày, gây viêm phúc mạc, đe dọa tính mạng.
- Ung thư dạ dày: H. pylori được Tổ chức Y tế Thế giới (WHO) xếp vào nhóm tác nhân gây ung thư dạ dày loại I. Cơ chế sinh ung thư liên quan đến quá trình viêm mạn tính kéo dài, dẫn đến biến đổi dị sản ruột, loạn sản và cuối cùng là ung thư biểu mô tuyến dạ dày. Đặc biệt, sự hiện diện của gen CagA làm tăng nguy cơ tiến triển thành ung thư do tác động mạnh lên các con đường tín hiệu tế bào, thúc đẩy tăng sinh và ức chế quá trình chết tế bào.
- Lymphoma MALT (Lymphoma mô lympho liên kết niêm mạc): Đây là một dạng ung thư hiếm gặp nhưng có liên quan chặt chẽ đến nhiễm H. pylori kéo dài. Sự kích thích liên tục của vi khuẩn lên mô lympho tại niêm mạc dạ dày dẫn đến tăng sinh bất thường tế bào lympho B, hình thành khối u ác tính. Đáng chú ý, điều trị tiệt trừ H. pylori có thể giúp thuyên giảm hoặc khỏi hoàn toàn lymphoma MALT giai đoạn sớm.
Ngoài các biến chứng chính trên, nhiễm H. pylori còn có thể liên quan đến một số bệnh lý ngoài dạ dày như thiếu máu thiếu sắt không rõ nguyên nhân, giảm tiểu cầu miễn dịch, các bệnh lý tự miễn và thậm chí là tăng nguy cơ mắc bệnh tim mạch do tác động gián tiếp qua phản ứng viêm toàn thân.
Việc phát hiện và điều trị sớm nhiễm H. pylori có ý nghĩa quan trọng trong phòng ngừa các biến chứng nguy hiểm, bảo vệ sức khỏe hệ tiêu hóa và nâng cao chất lượng cuộc sống cho người bệnh.
Chẩn Đoán Nhiễm Virus HP Dạ Dày
Các Phương Pháp Xét Nghiệm Hiện Đại
Nhiễm Helicobacter pylori (H. pylori) là một trong những nguyên nhân hàng đầu gây viêm loét dạ dày, ung thư dạ dày và các bệnh lý tiêu hóa mạn tính. Việc chẩn đoán chính xác nhiễm H. pylori đóng vai trò then chốt trong điều trị và phòng ngừa biến chứng. Hiện nay, các phương pháp xét nghiệm hiện đại được chia thành hai nhóm chính: không xâm lấn và xâm lấn, mỗi nhóm có ưu nhược điểm riêng, phù hợp với từng đối tượng bệnh nhân và mục đích lâm sàng.
- Test hơi thở ure (Urea breath test – UBT): Đây là phương pháp không xâm lấn được đánh giá là tiêu chuẩn vàng trong chẩn đoán nhiễm H. pylori hiện nay. Nguyên lý dựa trên khả năng tiết men urease mạnh của H. pylori. Bệnh nhân uống dung dịch chứa ure đánh dấu đồng vị (thường là 13C hoặc 14C). Nếu có H. pylori trong dạ dày, men urease sẽ phân giải ure thành amoniac và khí CO2 đánh dấu, được hấp thu vào máu và thải ra ngoài qua phổi. Khí CO2 này được thu thập và phân tích bằng máy chuyên dụng.
- Ưu điểm: Độ nhạy và độ đặc hiệu cao (trên 95%), không gây đau, an toàn cho cả trẻ em và phụ nữ mang thai.
- Nhược điểm: Cần nhịn ăn trước khi làm test, không sử dụng kháng sinh, bismuth hoặc thuốc ức chế bơm proton (PPI) ít nhất 2 tuần trước xét nghiệm để tránh âm tính giả.
- Ứng dụng: Chẩn đoán ban đầu, đánh giá hiệu quả điều trị tiệt trừ H. pylori sau khi kết thúc phác đồ.
- Xét nghiệm phân (H. pylori Stool Antigen Test): Phương pháp này phát hiện kháng nguyên H. pylori trong mẫu phân của bệnh nhân thông qua kỹ thuật miễn dịch enzyme (ELISA) hoặc sắc ký miễn dịch. Đây là xét nghiệm không xâm lấn, phù hợp với mọi lứa tuổi, đặc biệt hữu ích ở trẻ nhỏ.
- Ưu điểm: Độ nhạy và độ đặc hiệu cao (trên 90%), dễ thực hiện, không gây khó chịu cho bệnh nhân.
- Nhược điểm: Kết quả có thể bị ảnh hưởng nếu bệnh nhân đang dùng kháng sinh, bismuth hoặc PPI. Cần bảo quản mẫu phân đúng quy trình để đảm bảo độ chính xác.
- Ứng dụng: Chẩn đoán ban đầu, theo dõi sau điều trị tiệt trừ H. pylori.
- Xét nghiệm máu (Serology): Xét nghiệm huyết thanh học nhằm phát hiện kháng thể IgG kháng H. pylori trong máu. Đây là phương pháp không xâm lấn, thực hiện đơn giản, nhanh chóng.
- Ưu điểm: Dễ thực hiện, không bị ảnh hưởng bởi tình trạng dùng thuốc, phù hợp với các nghiên cứu dịch tễ học.
- Nhược điểm: Không phân biệt được nhiễm H. pylori hiện tại hay đã từng nhiễm trong quá khứ, do kháng thể tồn tại lâu trong máu sau khi đã tiệt trừ vi khuẩn. Độ nhạy và đặc hiệu thấp hơn so với các phương pháp khác.
- Ứng dụng: Sàng lọc cộng đồng, hỗ trợ chẩn đoán trong trường hợp không thể thực hiện các xét nghiệm khác.
- Nội soi dạ dày – sinh thiết (Invasive Tests): Đây là nhóm phương pháp xâm lấn, thường chỉ định khi bệnh nhân có triệu chứng nghi ngờ biến chứng hoặc thất bại với các phác đồ điều trị trước đó. Trong quá trình nội soi, bác sĩ lấy mẫu mô niêm mạc dạ dày để tiến hành các xét nghiệm chuyên sâu:
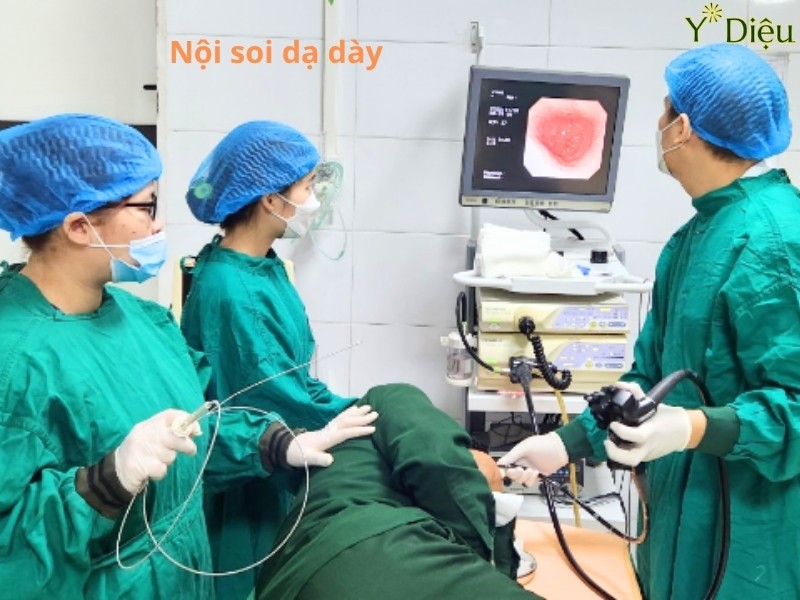
Nội soi dạ dày – sinh thiết cho kết quả nhanh chính xác
- Nhuộm soi mô học: Mẫu mô được nhuộm đặc biệt (Giemsa, Warthin-Starry, Hematoxylin-Eosin) để quan sát trực tiếp vi khuẩn dưới kính hiển vi. Độ nhạy và đặc hiệu cao, giúp đánh giá tổn thương mô học đi kèm (viêm, loét, dị sản, ung thư hóa).
- Test urease nhanh (Rapid Urease Test – RUT): Mẫu mô được đặt vào môi trường chứa ure và chất chỉ thị màu. Nếu có H. pylori, men urease sẽ phân giải ure, làm đổi màu môi trường. Kết quả có thể có sau 1–24 giờ.
- Nuôi cấy vi khuẩn: Mẫu mô được nuôi cấy trên môi trường đặc biệt để phân lập H. pylori. Đây là phương pháp duy nhất cho phép làm kháng sinh đồ, xác định chủng kháng thuốc, tuy nhiên kỹ thuật phức tạp, thời gian lâu (3–7 ngày), độ nhạy thấp do vi khuẩn khó nuôi cấy.
- Xét nghiệm sinh học phân tử (PCR): Phát hiện DNA của H. pylori trong mẫu mô bằng kỹ thuật khuếch đại gen (PCR). Độ nhạy và đặc hiệu rất cao, có thể phát hiện các đột biến gen liên quan đến kháng thuốc (như kháng clarithromycin, levofloxacin).
- Ưu điểm: Độ chính xác cao, cho phép đánh giá tổn thương niêm mạc, phát hiện biến chứng ác tính, xác định kiểu gen và tình trạng kháng thuốc của vi khuẩn.
- Nhược điểm: Xâm lấn, có thể gây khó chịu, đau, chảy máu hoặc nhiễm trùng; chi phí cao hơn; không phù hợp với bệnh nhân chống chỉ định nội soi.
- Ứng dụng: Chỉ định trong các trường hợp nghi ngờ ung thư dạ dày, loét phức tạp, thất bại điều trị hoặc cần xác định kháng thuốc.
So sánh các phương pháp chẩn đoán H. pylori:
| Phương pháp | Độ nhạy (%) | Độ đặc hiệu (%) | Không xâm lấn | Ứng dụng |
|---|---|---|---|---|
| Test hơi thở ure | 95–98 | 95–98 | Có | Chẩn đoán, theo dõi sau điều trị |
| Xét nghiệm phân | 90–95 | 90–95 | Có | Chẩn đoán, theo dõi sau điều trị |
| Xét nghiệm máu | 80–85 | 75–80 | Có | Sàng lọc, hỗ trợ chẩn đoán |
| Nội soi – sinh thiết | 90–99 | 90–99 | Không | Chẩn đoán, đánh giá biến chứng, kháng thuốc |
Việc lựa chọn phương pháp xét nghiệm phù hợp dựa trên tình trạng lâm sàng, khả năng tiếp cận kỹ thuật, chi phí và mục đích chẩn đoán. Trong thực hành, các bác sĩ thường phối hợp nhiều phương pháp để tăng độ chính xác, đặc biệt ở những trường hợp nghi ngờ hoặc thất bại điều trị. Ngoài ra, các xét nghiệm hiện đại như PCR còn giúp phát hiện sớm các chủng H. pylori kháng thuốc, hỗ trợ cá thể hóa phác đồ điều trị, giảm nguy cơ tái phát và biến chứng lâu dài.
Điều Trị Và Phòng Ngừa Virus HP Dạ Dày
Phác Đồ Điều Trị Tiêu Chuẩn
Nhiễm Helicobacter pylori (H. pylori) là nguyên nhân hàng đầu gây viêm loét dạ dày-tá tràng và ung thư dạ dày. Việc điều trị H. pylori đòi hỏi sự phối hợp nhiều loại kháng sinh nhằm tiêu diệt hoàn toàn vi khuẩn, đồng thời sử dụng thuốc ức chế bơm proton (PPI) để giảm tiết acid, tạo môi trường thuận lợi cho niêm mạc dạ dày hồi phục. Lựa chọn phác đồ điều trị cần dựa trên tình hình kháng thuốc tại địa phương, tiền sử dùng kháng sinh của bệnh nhân và các yếu tố nguy cơ cá nhân.

Cao dạ cẩm có thể ức chế và tiêu diệt Hp
- Phác đồ ba thuốc: Đây là lựa chọn đầu tay tại nhiều quốc gia, đặc biệt khi tỷ lệ kháng clarithromycin dưới 15%. Phác đồ gồm:
- Thuốc ức chế bơm proton (PPI): omeprazole, esomeprazole, lansoprazole hoặc pantoprazole, liều chuẩn 2 lần/ngày.
- Clarithromycin: 500 mg x 2 lần/ngày.
- Amoxicillin: 1g x 2 lần/ngày hoặc metronidazole: 500 mg x 2 lần/ngày (nếu dị ứng penicillin).
- Phác đồ bốn thuốc có bismuth: Được khuyến cáo khi thất bại với phác đồ ba thuốc hoặc tại vùng có tỷ lệ kháng clarithromycin cao. Thành phần gồm:
- PPI: liều chuẩn 2 lần/ngày.
- Bismuth subcitrate/subsalicylate: 120 mg x 4 lần/ngày.
- Tetracycline: 500 mg x 4 lần/ngày.
- Metronidazole: 500 mg x 3-4 lần/ngày.
- Phác đồ nối tiếp hoặc luân phiên: Áp dụng tại các khu vực có tỷ lệ kháng thuốc cao hoặc khi thất bại với các phác đồ truyền thống.
- Phác đồ nối tiếp: 5 ngày đầu dùng PPI + amoxicillin, 5-7 ngày tiếp theo dùng PPI + clarithromycin + metronidazole.
- Phác đồ luân phiên: 7 ngày đầu dùng PPI + amoxicillin, 7 ngày sau dùng PPI + clarithromycin + metronidazole.
Chú ý chuyên môn:
- Việc lựa chọn phác đồ cần dựa trên tình trạng kháng kháng sinh tại địa phương, tiền sử dị ứng thuốc và các bệnh lý nền của bệnh nhân.
- Khuyến cáo không tự ý mua thuốc điều trị mà cần có chỉ định và theo dõi của bác sĩ chuyên khoa tiêu hóa.
- Tuân thủ liều lượng, thời gian dùng thuốc là yếu tố quyết định thành công điều trị. Việc ngừng thuốc sớm hoặc dùng không đủ liều làm tăng nguy cơ kháng thuốc và tái phát.
- Sau điều trị, cần kiểm tra lại bằng các phương pháp như test hơi thở ure, test phân tìm kháng nguyên H. pylori hoặc nội soi sinh thiết để xác nhận đã diệt trừ hoàn toàn vi khuẩn.
- Không nên kiểm tra lại quá sớm (trước 4 tuần sau khi kết thúc điều trị), tránh kết quả âm tính giả do tác động của thuốc.
| Phác đồ | Thành phần | Thời gian | Hiệu quả (%) |
|---|---|---|---|
| Ba thuốc | PPI + Clarithromycin + Amoxicillin/Metronidazole | 10-14 ngày | 70-85 |
| Bốn thuốc có bismuth | PPI + Bismuth + Tetracycline + Metronidazole | 10-14 ngày | 85-90 |
| Nối tiếp/Luân phiên | PPI + Amoxicillin (5-7 ngày), sau đó PPI + Clarithromycin + Metronidazole (5-7 ngày) | 10-14 ngày | 80-90 |
Tác dụng phụ thường gặp: rối loạn tiêu hóa, dị ứng thuốc, vị kim loại trong miệng, tiêu chảy, buồn nôn. Nếu xuất hiện triệu chứng nặng, cần liên hệ bác sĩ để được tư vấn kịp thời.
Biện Pháp Phòng Ngừa Lây Nhiễm HP Dạ Dày
H. pylori lây truyền chủ yếu qua đường miệng - miệng, phân - miệng hoặc qua nguồn nước, thực phẩm bị ô nhiễm. Việc phòng ngừa lây nhiễm không chỉ giúp bảo vệ cá nhân mà còn góp phần giảm tỷ lệ mắc bệnh trong cộng đồng. Các biện pháp phòng ngừa hiệu quả bao gồm:
- Vệ sinh cá nhân:
- Rửa tay sạch bằng xà phòng trước khi ăn và sau khi đi vệ sinh.
- Giữ móng tay ngắn, sạch sẽ, tránh đưa tay lên miệng.
- Ăn chín uống sôi:
- Không ăn thực phẩm sống, tái, chưa được nấu chín kỹ.
- Uống nước đã đun sôi hoặc nước đóng chai đảm bảo vệ sinh.
- Tránh dùng chung vật dụng cá nhân:
- Không dùng chung bát đũa, cốc chén, khăn mặt, bàn chải đánh răng với người khác, đặc biệt là người có nguy cơ hoặc đã nhiễm H. pylori.
- Đảm bảo nguồn nước sạch, an toàn thực phẩm:
- Chọn mua thực phẩm tươi, rõ nguồn gốc, rửa sạch trước khi chế biến.
- Bảo quản thực phẩm đúng cách, tránh nhiễm khuẩn chéo.
- Khám sức khỏe định kỳ, tầm soát H. pylori:
- Đặc biệt ở những người có yếu tố nguy cơ như tiền sử gia đình ung thư dạ dày, viêm loét dạ dày-tá tràng, hoặc có triệu chứng nghi ngờ (đau thượng vị, đầy hơi, buồn nôn kéo dài).
- Thực hiện các xét nghiệm chẩn đoán như test hơi thở ure, test phân tìm kháng nguyên H. pylori, nội soi dạ dày khi có chỉ định.
- Nâng cao nhận thức cộng đồng:
- Tuyên truyền về nguy cơ lây nhiễm, tác hại của H. pylori và các biện pháp phòng tránh trong trường học, nơi làm việc, gia đình.
- Khuyến khích chủ động đi khám khi có triệu chứng tiêu hóa kéo dài.
Lưu ý chuyên sâu:
- Hiện nay, chưa có vaccine phòng ngừa H. pylori. Phòng bệnh chủ yếu dựa vào vệ sinh cá nhân và an toàn thực phẩm.
- Trẻ em là đối tượng dễ nhiễm H. pylori do thói quen sinh hoạt, ăn uống chung và hệ miễn dịch chưa hoàn thiện.
- Việc điều trị triệt để cho các thành viên trong gia đình có người nhiễm H. pylori giúp giảm nguy cơ tái nhiễm.
- Không nên tự ý sử dụng kháng sinh để phòng ngừa, tránh làm tăng tình trạng kháng thuốc trong cộng đồng.